|
Document sans titre
I] Principes de la radioactivité :
1) Historique :
La radioactivité a été découverte en 1896 par Henry Becquerel Lequel, suivant une suggestion de H. Poincaré, cherchait si les corps fluorescents émettaient un rayonnement susceptible d’impressionner la plaque photographique à travers un papier noir. Becquerel fît ses expériences avec des sels d’Uranium qu’il exposait au soleil pour les rendre fluorescents. Les résultats furent positifs : mais, lorsque par manque de soleil, il laissa au voisinage d’une plaque photographique un sel d’uranium, il constata que la plaque était tout de même impressionnée, il admit que l’Uranium émet des rayonnements particuliers qu’on appela « rayons uraniques »
Dès Juillet 1898 avec son mari Pierre, Marie Curie annonçait la présence d’un nouvel élément : le Polonium ( Z=84),
C’est ensuite avec Bemont, en Décembre 1898, qu’ils découvrent l’existence du Radium ( Z= 88), c’est alors qu’elle proposa le nom de radioactivité au phénomène découvert par Becquerel.
Par la suite, de très nombreuses expériences furent entreprises pour déterminer les lois de la radioactivité et découvrir de nouveaux éléments .
Henry Becquerel, photographie |

Marie Curie ,photographie |
2) Définition :
a)définition
On appelle radioactivité la transformation spontanée d’un noyau atomique au cours de laquelle ce dernier émet un rayonnement .
L’observation des effets de ce rayonnement a conduit à la découverte de la radioactivité et des radio-élements. On classe ainsi les éléments présents dans la nature en 2 catégories :
- Ceux dont les noyaux ne subissent au cours du temps aucun transformation (éléments stables)
- Ceux dont les noyaux émettent un rayonnement au cour de leur existence (éléments radioactifs)
Parmi les 92 éléments naturels dénombrés, une douzaine sont radioactifs.
En effet, la grande majorité des noyaux que l'on trouve dans la nature sont stables, les autres ayant disparu. Les seuls noyaux encore présents dans la nature sont ceux possédant une durée de vie très longue (par exemple l'uranium ou le thorium) ou ceux qui sont renouvelés en permanence (par exemple le carbone-14 ou le tritium qui sont renouvelés sous l'effet des rayonnements cosmiques entrant dans l'atmosphère).
b)Ce tableau périodique montre quels sont les éléments radioactifs :

Il est important de préciser qu'il existe de nombreux isotopes radioactifs autres que les radioéléments représentés ici. Le carbone, par exemple possède des isotopes radioactifs ( Le carbone-14, par exemple), mais l'isotope le plus fréquemment rencontré dans la nature, le carbone-12 est stable. C'est pour cette raison que le carbone est cité ici comme un élément stable.
c) Les Familles radioactives
Chaque désintégration d'un élément radioactif provoque sa transformation en un nouvel élément (transmutation à la suite de l'émission d'une particule) Tous les radio-isotopes radioactifs appartiennent à une famille radioactive. Ces familles marquent l'évolution des éléments radioactifs. Les ancêtres de ses familles qui existent au nombre de trois sont le thorium-232, l'actinium-uranium-235 et l'uranium-238. Elles sont constituées d'une trentaine d'éléments de nombre de masse compris entre 206 et 238. Ces trois noyaux radioactifs étaient déjà présents dans les nuages de poussières cosmiques apparus à la suite de l'explosion des supernovae. Ces nuages de poussière sont à l'origine de la terre. L'élément final est stable. Il est dans les trois cas un isotope de l'élément plomb.
d)Carte des types de désintégrations

Cette carte représente tous les isotopes existant. Ils sont classés en fonction de leur nombre de neutrons (en abscisse) et de leurs protons (en ordonnée). On constate la présence d'une " vallée de stabilité ", en noir, constituée par les noyaux stables, contenant protons et neutrons en proportion idéale. On remarque aussi que les noyaux contenant un excédent de neutrons (en bleu) ont tendance à essayer d'atteindre la stabilité par des désintégrations β - et ceux contenant un excédent de protons par des désintégration β + (en orange). Les noyaux les plus lourds, en haut à droite, ont eux tendance à réduire leur masse par des désintégrations α. De plus, on constate la présence de cas extrêmes : les noyaux avec une proportion de protons trop grande, en éjectent directement (en rouge), il en est de même pour les neutrons (en violet) et pour les noyaux extrêmement lourds qui fissionnent (se cassent en deux) de façon spontanée.
3) Mécanismes :
La radioactivité affecte les noyaux de plus de 72 protons car les forces d’interactions électriques l’emportent sur l’interaction forte qui maintenait la cohésion du noyau.
Les noyaux doivent leur stabilité à la force attractive nucléaire (interactions fortes) qui l'emporte sur la répulsion entre les charges électriques de même signe des protons. Cette attraction requiert un équilibre entre les protons et les neutrons. Pour assurer cet équilibre intervient une troisième force, appelée " interaction faible ", qui agit au sein même des nucléons et a la capacité de transformer neutrons en protons et vice-versa. Soumis à ces forces, les noyaux naturels évoluent constamment vers la stabilité en se transformant : ces transformations constituent la radioactivité.
“Selon les noyaux, la radioactivité dure quelques secondes, plusieurs jours ou des milliards d’années.”
a)la décroissante radioactive :
L’activité d’un échantillon radioactif diminue avec le temps du fait de la disparition progressive des noyaux instables qu’il contient. La désintégration radioactive d’un noyau donné est un phénomène aléatoire.
On peut cependant donner pour chaque isotope radioactif une période radioactive ou demi-vie qui est le temps au bout duquel la moitié des atomes radioactifs initialement présents a disparu par transformation spontanée.
Selon les noyaux radioactifs concernés, cette période est très variable : quelques secondes, heures… plusieurs jours… centaines d’années… ou milliards d’années.
b) les différents types de désintégrations
Radioactivité alpha
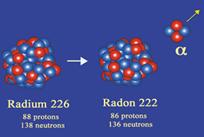
La radioactivité alpha concerne les gros noyaux, dont le plus gros observé dans la nature est celui de l'uranium-238 comportant 92 protons et 136 neutrons. De tels noyaux, instables, émettent un noyau léger d'hélium (Z=2) afin de devenir moins volumineux et ainsi se rapprocher de la stabilité. Il s'avère que cette manière d'expulser deux protons et deux neutrons groupés est plus économique que d'expulser des protons et des neutrons de manière isolée.
L'énergie libérée lors d'une désintégration alpha se retrouve sous forme d'énergie cinétique partagée entre la particule α et le noyau. Comme dans un tir d'artillerie où l'obus emporte pratiquement toute l'énergie de la déflagration, les particules α emportent environ 98 % de l'énergie. L'énergie de la particule alpha est unique pour une désintégration donnée. Elle est de l'ordre de quelques Mev (millions d'électronvolts), ce qui est assez considérable pour une seule particule.
Les périodes des désintégrations alpha sont souvent longues. Ainsi, certains émetteurs alpha comme le thorium-232 et l'uranium-238 mettent des milliards d'années à se désintégrer. Le radium-226 se désintègre lui avec une période de 1600 ans.
Equation d'une désintégration α :

Un noyau de nature X se désintègre en un noyau de type Y avec deux neutrons et deux protons en moins en émettant une particule alpha (noyau d'hélium) et un photon α.
Exemple de la désintégration du Radium 226
La radioactivité Bêta-, Bêta+ et la capture électronique :
Ces 3 modes de transformation sont caractérisés par le fait que le numéro atomique Z du noyau radioactif change d’une unité sans variation du nombre de masse A
Radioactivité bêta moins
Certains atomes dont les noyaux sont trop chargés en neutrons émettent un rayonnement bêta moins. Un des neutrons au sein du noyau se désintègre en un proton plus un électron chargé négativement, et d’un antineutrino (dont la détection est très difficile), ces deux derniers étant éjectés. Ainsi l’atome s’est transformé en un autre élément chimique. Par exemple, le thorium 234 est radioactif bêta moins et se transforme en protactinium 234.
Equation de la désintégration β -:

L'énergie de la désintégration se partage entre : le noyau qui recule, l'électron (ou le positon) et l'antineutrino (ou le neutrino). Le noyau, bien plus lourd que les deux autres participants, n'emporte pratiquement pas d'énergie.
L'excès de neutrons étant fréquent parmi les noyaux radioactifs naturels, la radioactivité β - est de loin la plus observée dans la nature.
Radioactivité bêta +
Certains atomes dont les noyaux sont trop chargés en protons émettent un rayonnement bêta plus. Un des protons au sein du noyau se désintègre en un neutron plus un positon (particule de même masse que l’électron mais chargée positivement), ce dernier étant éjecté ainsi qu’un neutrino. Ainsi l’atome s’est transformé en un autre élément chimique. Par exemple, l’iode 122 est un radioactif bêta plus et se transforme en tellure 122.
Equation de la désintégration β+

Les deux types de désintégration β

la capture électronique
La capture électronique est un processus par lequel le noyau radioactif se saisi d’un électrons de son cortège en émettant un neutrino n .L’observation de cette transformation est plus délicate puisque le rayonnement d’origine nucléaire et très difficile à mettre en évidence
La fission spontanée
.Pour les éléments très lourds ( Z > 90 ), les noyaux on une probabilité mesurable de subir spontanément la fission, phénomène par lequel le noyau se scinde en 2 fragments sensiblement égaux.
Radioactivité gamma γ
Le rayonnement gamma est une onde électromagnétique comme la lumière visible ou les rayons X mais plus énergétique.
Ce rayonnement suit souvent une désintégration alpha ou bêta. Après émission de la particule alpha ou bêta, le noyau est encore excité car ses protons et ses neutrons n’ont pas trouvé leur équilibre. Il se libère alors rapidement d’un trop-plein d’énergie par émission d’un rayonnement gamma. C’est la radioactivité gamma. Par exemple, le cobalt 60 se transforme par désintégration bêta en nickel 60 qui atteint un état stable en émettant un rayonnement gamma.
Emission d'un rayon gamma

Dans cette illustration, le noyau possède un excédent d'énergie : il est déformé et animé d'une rotation autour d'un axe. Il retrouve ensuite une forme sphérique et perd sa rotation en émettant une radiation gamma qui emporte l'excédent d'énergie.
4) Les unités de mesure
Unités de la Radioactivité
ACTIVITÉ NUCLÉAIRE |
Multiples et sous-multiples usuels |
Dénomination |
Définition |
Dénominations |
Valeur |
Symbole |
becquerel |
Activité nucléaire d'une quantité de radioélément (ou nucléide radioactif) pour laquelle le nombre de désintégrations par seconde est 1. |
becquerel |
2,7027.10-11 Ci |
Bq |
curie |
3,7.1010 Bq |
Ci |
millicurie |
10-3 Ci |
mCi |
|
|
|
Unités d'activité nucléaire américaines ou anglaises |
Désignation |
Abrév. |
Relations |
Valeurs, concordances et remarques |
rutherfords |
Ru |
|
2,7.10-17 Ci |
QUANTITÉ de RAYONNEMENT X ou g |
Multiples et sous-multiples usuels |
Dénomination |
Définition |
Dénominations |
Valeur |
Symbole |
röntgen |
Quantité de rayonnement X ou gamma telle que l'émission corpusculaire qui lui est associée dans 0,001293 gramme d'air produise, dans l'air, des ions transportant une quantité d'électricité, de l'un ou l'autre signe, égale à 1/3.109 coulomb. |
röntgen |
|
R |
N'est plus autorisé par décret 2003-165 du 27 février 2003.
|
|
|
DOSE ABSORBÉE, KERMA |
Multiples et sous-multiples usuels |
Dénomination |
Définition |
Dénominations |
Valeur |
Symbole |
coulomb par kilogramme |
Unité d'exposition. |
coulomb par kilogramme |
3876 röntgen |
C/kg |
de par sa référence au röntgen.
|
|
|
sievert |
Unité d'équivalent de dose (produit de la dose absorbée par le facteur de qualité Q qui rend compte de l'effet biologique, différent selon la nature du rayonnement) |
sievert |
|
Sv |
rem |
10-2 Sv |
rem |
Anciennement rem (röntgen equivalent for man).
Le sievert est l'équivalent d'un joule par kilogramme. |
gray |
Unité de dose absorbée ou Kerma dans une masse de matière de 1 kg à laquelle les rayonnements ionisants communiquent une énergie de 1 joule. |
gray |
|
Gy |
rad |
10-2 Gy |
rad |
|
schema de la pénétration des differents rayonnements :

|



 -Historique
-Historique Lexique
Lexique